Glukokortikoid induzierte Osteoporose (GIOP)
Glukokortikoide werden auch heute noch oft zur Behandlung verschiedener entzündlicher und nicht-entzündlicher muskuloskelettaler Erkrankungen eingesetzt. Dabei ist Medizinern die „Steroid-Osteoporose“ als Komplikation gut bekannt, bei wiederholten Infiltrationen aber oft zu wenig bewusst. Insbesondere, wenn durch verschiedene Ärzte Glukokortikoide infiltriert werden, ist die Übersicht über die kumulativen Interventionen durch den Hausarzt entscheidend, um eine Osteoporoseabklärung einzuleiten und rechtzeitig eine entsprechende Prophylaxe oder Therapie zu etablieren. Diese ist oft bereits bei osteopenen Messwerten nötig.
Osteoporotische Frakturen sind häufig. In der Schweiz erleiden über 70'000 Personen pro Jahr eine osteoporosebedingte Fraktur. Glukokortikoide stellen die häufigste sekundäre Ursache für Osteoporose und durch Osteoporose bedingte Frakturen dar, was dem Thema Steroidosteoporose (oder Glukokortikoid-induzierte Osteoporose, kurz GIOP) ein besonderes Gewicht gibt. Der folgende Ratgeber erläutert, wann an eine Steroidosteoporose gedacht und eine entsprechende Abklärung eingeleitet werden soll und welche therapeutischen Optionen bestehen.
GIOP - Häufig vergessen, von Beginn weg ein Risiko
Trotz des klar belegten Zusammenhangs zwischen Glukokortikoiden und Osteoporose bleiben entsprechende Abklärungen und Therapien oft aus. So zeigen verschiedene Untersuchungen, dass nur ein Bruchteil der Patienten und Patientinnen, welche längerfristig (>3 Monate) Glukokortikoide bekamen, eine entsprechende Abklärung und Therapie erhielten[1]. Der negative Effekt auf den Knochen und das Frakturrisiko setzt schon unmittelbar bei Therapiebeginn ein, bleibt aber über die gesamte Dauer erhalten. Untersuchungen zeigen schon nach wenigen Wochen eine Zunahme der Zahl und Aktivität der Osteoklasten und eine Inaktivierung der Osteoblasten[2]. Hervorzuheben ist, dass bereits bei osteopenen Knochendichtewerten ein stark erhöhtes Frakturrisiko bestehen kann, obwohl formal/messtechnisch keine Osteoporose besteht.
Wann soll eine Weiterabklärung erfolgen?
Werden Glukokortikoide oral verabreicht, richten wir uns nach der Empfehlung der Schweizerischen Gesellschaft für Rheumatologie[3]: Bei einer Behandlung mit ≥ 5 mg Prednison-Äquivalent/Tag und einer voraussichtlichen Dauer von über 3 Monaten soll (möglichst innerhalb der ersten Wochen) eine Abklärung erfolgen. Bei injizierten Glukokortikoiden gelten die gleichen Grundsätze. Klare «Steroid-Äquivalenzen am Knochen» für verschiedene nicht oral applizierte Glukokortikoide und unterschiedliche Applikationsrouten (i.m., i.a., etc.) existieren nicht oder nur bedingt, wobei wir bei uns als Richtwert 4 x 40 mg Triamcinolonacetonid/Jahr festgelegt haben (natürlich in Abhängigkeit vom Grundrisikoprofil der Patienten für eine Osteoporose).
Abklärung und Interpretation
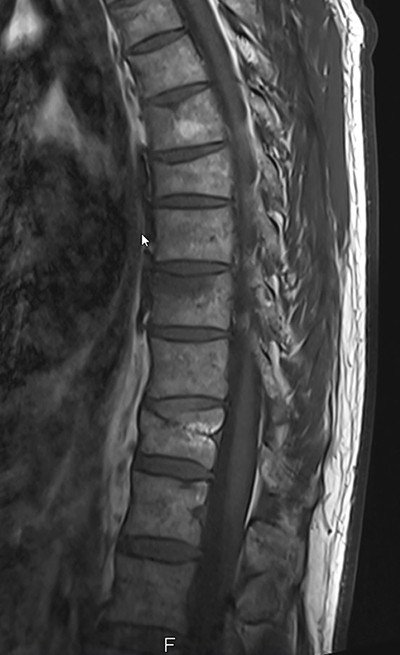
Die Abklärung erfolgt mittels Knochendichtemessung, wobei standardmässig eine DXA (dual-energy X-ray absorptiometry) durchgeführt wird. Die DXA wird nur unter gewissen Voraussetzungen (an nur einer Messregion) durch die Krankenkassen übernommen (Tabelle 1). Weiter ergänzen wir bei älteren Patienten oder Grössenverlust eine Morphometrie, um asymptomatische Wirbelkörperfrakturen nicht zu verpassen (gut 2/3 aller osteoporotischen Wirbelkörperfrakturen sind asymptomatisch!).
-
Indikationen für eine DXA, welche gemäss KVG übernommen werden
1. Manifeste Osteoporose (Fraktur bei inadäquatem Trauma, T-Score ≤ -2.5 in der DXA) 2. Verlaufskontrolle einer bekannten Osteoporose unter Therapie 3. Bei Langzeit-Glukokortikoidtherapie (meist definiert als ≥ 5mg Prednisonäquivalent/Tag über ≥ 3 Monate) 4. Bei gastrointestinalen Erkrankungen mit Malabsorption (St. n. Magenbypass-OP, M. Crohn, Zöliakie, Colitis ulcerosa) 5. Primärer Hyperparathyreoidismus ohne klare Operationsindikation 6. Osteogenesis imperfecta 7. HIV
Gemäss WHO definiert sich die Osteoporose entweder durch eine osteoporotische Fraktur oder durch den tiefsten T-Score von LWS (mindestens 2 benachbarte Wirbelkörper müssen beurteilbar sein), „Hüfte gesamt“ oder Schenkelhals. Bei Männern unter 50 Jahren und prämenopausalen Frauen sollte nicht der T-Score, sondern der Z-Score beurteilt werden. Dabei sollte nicht von Osteoporose/Osteopenie, sondern von «einer für das Alter und Geschlecht normalen (Z-Score bis -1.9) oder zu tiefen (Z-Score ≤ -2.0) Knochendichte» gesprochen werden. Tabelle 2 zeigt die entsprechenden Einteilungen. Zur Abschätzung des individuellen Frakturrisikos soll die Messung in ein Risiko-Assessment einfliessen (z. B. FRAX-Tool [4]).
-
Postmenopausale Frauen und Männer ≥ 50 Jahre
T-Score (DXA): Beurteilung: >-1.0 Normal -1.0 bis -2.5 Osteopenie ≤-2.5 Osteoporose Prämenopausale Frauen und Männer <50 Jahre
Z-Score (DXA): Beurteilung: >-1.9 Für Alter und Geschlecht normale Knochendichte ≤-2.0 Für Alter und Geschlecht zu tiefe Knochendichte
Allgemeine therapeutische bzw. prophylaktische Massnahmen
Wir empfehlen allen Patienten mit ≥ 5 mg Prednison-Äquivalent/Tag über eine voraussichtliche Dauer von ≥ 3 Monaten eine Supplementation mit Vitamin D (800 I.E./Tag) und Kalzium (je nach nutritiver Zufuhr; meist 500 mg/Tag zusätzlich). Wir sind uns aber bewusst, dass die Studienlage hierzu nicht abschliessend geklärt ist[5]. Neben der Erfassung und Reduktion des Sturzrisikos ist es wichtig, dass die Patienten möglichst körperlich aktiv bleiben. Vor allem auch Krafttraining hat einen positiven Effekt auf die Knochendichte.
Spezifische medikamentöse Therapie
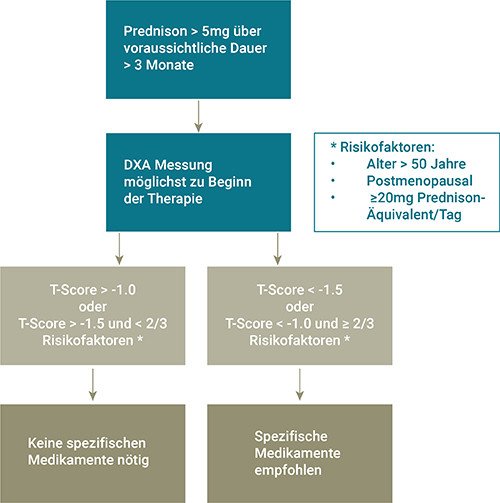
Für den Entscheid bezüglich Osteoporose-spezifischer Medikamente richten wir uns nach den Empfehlungen der Schweizerischen Gesellschaft für Rheumatologie, wie dies Abbildung 2 veranschaulicht [3], oder wir verwenden einen der Risiko-Scores (z. B. FRAX-Tool mit Anpassung).
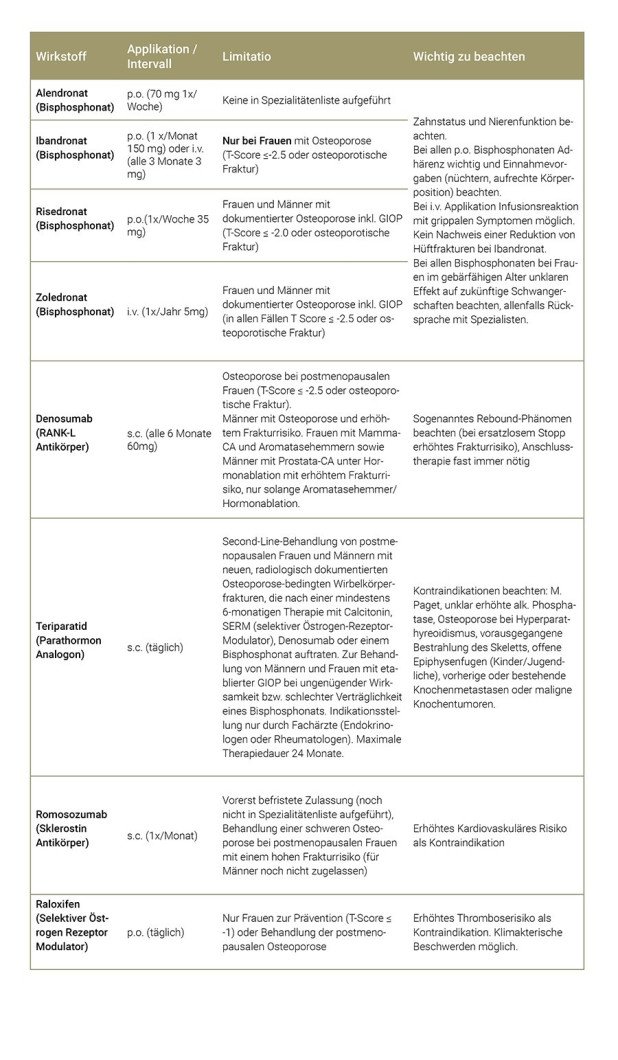
Primär kommen antiresorptive Medikamente in Frage und hier speziell die Bisphosphonate. Ohne Limitatio versehen ist nur Alendronat p.o. und stellt somit formal erste Wahl dar. Die restlichen Bisphosphonate und Denusomab (RANK-L -Antikörper) sind oft nur ausserhalb der Limitatio möglich, was allenfalls eine Kostengutsprache bedingt (siehe Tabelle 3). Die Limitatio und Zulassung (Label) ausser Acht gelassen, wäre eine medikamentöse Prophylaxe bzw. Therapie ideal, welche sowohl auf den Knochenaufbau als auch den -abbau wirkt und so den gesamten negativen Effekt der Glukokortikoide auf den Knochen adressiert. Bis vor kurzem waren Teriparatid und seine Biosimilars (Forsteo®, Terrosa®, Movymia®, Teriparatid MEPHA®) die einzigen verfügbaren osteoanabolen Medikamente. Dafür besteht auch eine Zulassung für Männer und Frauen, jedoch nur als Zweitlinientherapie zur Behandlung der GIOP (nach entsprechendem Kostengutsprachegesuch). Neu ist nun auch der Sklerostin-Antikörper Romosozumab (Evenity®) erhältlich, welcher sowohl osteoanabol als auch antiresorptiv wirksam ist. Theoretisch wäre dies ebenfalls ein guter Wirkansatz für die GIOP, wobei Studien hierzu noch fehlen, aber geplant sind. Ausserdem ist die Zulassung für dieses Präparat in der Schweiz noch befristet und vorerst auf postmenopausale Frauen mit schwerer Osteoporose und hohem Frakturrisiko limitiert.
Zusammenfassung
Zusammenfassend soll beim Einsatz von Glukokortikoiden immer von Beginn weg an die Möglichkeit einer GIOP gedacht werden, und zwar unabhängig von der Applikationsart (i.m., i.a., p.o.). Schon die Frühphase ist für den Knochen entscheidend, weshalb bereits bei Behandlungsbeginn an eine entsprechende Abklärung gedacht werden soll. Diese ist mit DXA und gesamtheitlicher Risikoabschätzung einfach umsetzbar, und es bestehen verschiedene medikamentöse und nicht-medikamentöse Prophylaxe- und Therapiemöglichkeiten. Bei der gezielten medikamentösen Behandlung müssen jedoch die jeweilige Limitatio bzw. Zulassungsindikation (Label) beachtet werden.
Quellen
- Frenkel B, White W, Tuckermann J. Glucocorticoid-Induced Osteoporosis. Adv Exp Med Biol. 2015;872:179-215. doi: 10.1007/978-1-4939-2895-8_8. PMID: 26215995; PMCID: PMC5905346.
- Adami G, Saag KG. Glucocorticoid-induced osteoporosis: 2019 concise clinical review. Osteoporos Int. 2019 Jun;30(6):1145-1156. doi: 10.1007/s00198-019-04906-x. Epub 2019 Feb 25. PMID: 30805679.
- https://www.rheuma-net.ch/de/fachinformationen/behandlungsempfehlungen
- https://www.sheffield.ac.uk/FRAX/tool.aspx?lang=de
- Buckley LM, Leib ES, Cartularo KS, Vacek PM, Cooper SM. Calcium and vitamin D3 supplementation prevents bone loss in the spine secondary to low-dose corticosteroids in patients with rheumatoid arthritis. A randomized, double-blind, placebo-controlled trial. Ann. Intern. Med.
Autor: Dr. Marco Etter, Oberarzt Rheumatologie und Rehabilitation